
华夏时报记者 于娜 北京报道
近日,美国食品药品监督管理局(FDA)正式发布早期预警,直指三诺生物旗下美国子公司Trividia Health(下称“Trividia”)部分血糖仪产品说明存在严重疏漏。这一预警迅速引发全球糖尿病患者及行业的关注,也让三诺生物这一国产血糖监测领域龙头企业的海外布局再度成为焦点。
此次预警核心指向Trividia旗下TRUE METRIX系列血糖仪的E-5错误代码指引问题,该疏漏可能导致用户误判极高血糖信号、延误治疗,截至2026年1月16日,全球已出现114例相关严重伤害报告、1例死亡报告。与此同时,Trividia已同步启动产品标签及使用说明更正工作,明确风险及应急处理方案。
作为三诺生物在2016年以近3亿美金收购的核心海外资产,Trividia是其全球化布局的关键棋子,此次事件恰逢三诺生物预计2025年净利润大幅下滑之际,不仅考验着企业的应急处置能力,也为其海外业务的稳健发展带来新的挑战。对于上述问题,《华夏时报》记者联系采访三诺生物,截至发稿未收到回复。
海外产品管控爆雷
作为美国市场主流血糖仪品牌,Trividia旗下的TRUE METRIX系列自2014年8月推出以来,迅速覆盖COSTCO开市客、Walmart沃尔玛等零售巨头,以及Walgreen等连锁药房,远销全球13个国家和地区,成为三诺生物海外收入的重要支撑。
而此次预警的核心,正是该系列血糖仪的E-5错误代码解读与操作指引存在疏漏。据FDA披露,当用户血糖值高达600毫克/分升以上(属于危及生命的极高血糖水平),或测试试纸出现错误时,设备都会弹出E-5错误代码。但原有使用说明并未清晰区分这两种情况,仅给出笼统的操作建议,未对极高血糖的风险进行重点警示,这就可能导致用户在出现该错误代码,并伴随疲劳、口渴、视力模糊、多尿等高血糖症状时,误将其当作设备故障处理,进而延误最佳治疗时机。
FDA在预警中指出,高血糖患者若延误治疗,可能引发脱水、意识异常等严重并发症,极端情况下会导致死亡。截至2026年1月16日的统计数据显示,自该系列产品上市以来,全球已收到114例相关严重伤害报告、1例死亡报告。
面对此次风险,Trividia已于2026年2月6日率先启动产品标签及使用说明更正工作。更新后的指引明确了E-5错误代码的应对方案:用户收到错误代码后,应先用新试纸重测;若错误持续且伴随高血糖症状,需立即就医;若无相关症状则再次重测,仍有错误可拨打客服求助。同时Trividia强调,涉事血糖仪本身无质量问题,无需退回、更换,也无需下架,仅需更正使用说明即可,以此缓解用户恐慌情绪。
三诺生物也在媒体采访时补充回应,TRUE METRIX系列血糖仪未在中国市场销售,国内销售的其他产品无需进行相应更正,不会对国内用户造成影响,且此次预警是基于子公司主动更新产品说明作出,并非产品质量事故。
业绩承压雪上加霜
此次FDA预警事件的发生,恰逢三诺生物业绩面临较大压力的关键时期。就在FDA发布预警前夕,三诺生物披露了2025年度业绩预告,显示公司当期净利润为正值,但同比下滑幅度超过50%,而其核心海外子公司Trividia的相关支出,正是导致业绩下滑的诱因之一。
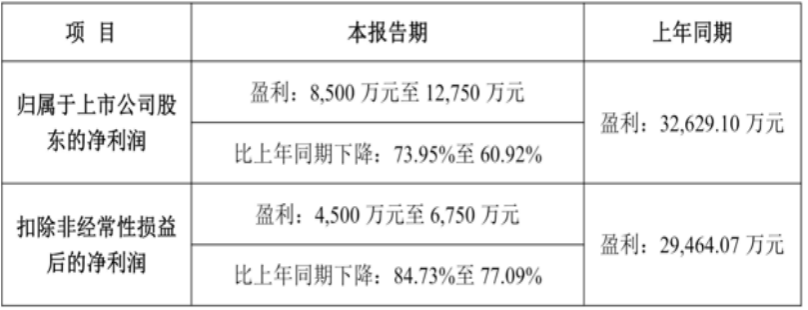 (来源:三诺生物2025年业绩预告)
(来源:三诺生物2025年业绩预告)公开资料显示,三诺生物自2002年创立以来,专注于生物传感技术研发,聚焦慢性疾病快速检测产品,从血糖监测领域起步,经过二十多年的发展,已成为国产血糖监测领域的领先企业,占据我国50%以上的血糖仪零售市场。2016年1月28日,三诺生物在长沙完成对Trividia的收购交割,收购金额高达27250万美元(约合近20亿元人民币),创下当时中国医疗器械行业海外并购的最高纪录。
此次收购,成为三诺生物全球化布局的关键性一步。凭借Trividia在北美市场的成熟渠道和品牌影响力,三诺生物迅速打开欧美市场,逐步实现全球市场的全面布局,如今已成长为全球第四大血糖仪企业,稳固跻身全球领先阵营,海外业务也成为公司业绩增长的核心驱动力。
但这份亮眼的海外布局背后,却暗藏业绩隐忧。据三诺生物2025年度业绩预告,2025年1—12月,公司归属于上市公司股东的净利润预计为8500万元至12750万元,较上年同期的32629.10万元下降73.95%至60.92%;扣非后净利润预计为4500万元至6750万元,较上年同期的29464.07万元下降84.73%至77.09%,下滑幅度显著。
三诺生物在业绩预告中表示,业绩下滑主要受三大因素影响,其中两项均与海外子公司直接相关。一是Trividia与罗氏就BGM产品达成专利交叉许可和解,需向罗氏净额支付1900万美元,这一支出直接影响公司净利润约7463万元,而这也是2025年三季度三诺生物净利润受到影响的重要原因之一;二是另一家子公司PTS公司业绩未达预期,公司拟计提商誉减值13000万元至17000万元,进一步侵蚀净利润;三是公司加大CGM(连续血糖监测系统)、BGM(指尖血糖监测)新品投放力度,产品结构变化影响毛利率,同时行业竞争加剧导致市场费用增加,多重因素叠加,导致公司业绩出现大幅下滑。
此次FDA预警事件,无疑让三诺生物的业绩压力雪上加霜。尤其是在血糖仪行业召回频发、专利大战愈演愈烈的背景下,三诺生物的海外布局面临着多重挑战。
当前,全球血糖仪品牌召回事件频发,且多为行业头部企业:2026年1月,雅培旗下部分FreeStyle Libre 3 / 3 Plus CGM被FDA列为Class I级(最高级别)召回,使用该设备可能导致严重伤害或死亡;2025年9月,安晟信因血糖仪读数单位设置错误,对其CONTOUR NEXT GEN meter血糖仪启动二级主动召回,涉事产品未进口至中国,凸显出血糖仪行业在产品细节管控上的普遍短板。
与此同时,血糖仪行业的专利大战也全面打响。除了Trividia与罗氏的专利和解,三诺生物目前仍与雅培围绕CGM产品展开专利诉讼,海牙UPC分院曾驳回雅培的临时禁令申请,但双方均可上诉,纠纷仍在持续。此外,硅基仿生、微泰医疗等其他国产血糖仪企业,也曾遭雅培在欧洲等地发起专利起诉,专利纠纷已成为国产企业出海的重要阻碍。
“此次FDA预警事件既是一次危机,也是一次反思和优化的契机。”医健管理咨询合伙人曹宁向《华夏时报》记者表示,作为国产医疗器械出海的标杆企业,三诺生物的海外布局之路,不仅关乎自身业绩增长,也为其他国产企业提供了借鉴。在同质化竞争加剧、技术迭代加速、监管日趋严格的背景下,企业既要加大研发投入、突破专利壁垒,也要重视产品细节管控和使用说明的规范性,完善上市后风险监测体系,才能在全球市场实现长期稳健发展。
责任编辑:姜雨晴 主编:陈岩鹏



 微信扫一扫打赏
微信扫一扫打赏
 支付宝扫一扫打赏
支付宝扫一扫打赏





